Testsealabs 猴痘病毒(MPV)核酸检测试剂盒
预期用途
| 检测类型 | 咽拭子和鼻拭子 |
| 测试类型 | 定性 |
| 测试材料 | 聚合酶链反应 |
| 包装尺寸 | 48次测试/1盒 |
| 储存温度 | 2-30℃ |
| 保质期 | 10个月 |
产品特点
原则
本试剂盒以MPV f3L基因特异保守序列为靶区域,采用实时荧光定量PCR技术及核酸快速释放技术,通过扩增产物荧光信号的变化来监测病毒核酸。检测体系包含内部质控,用于监测样本中是否存在PCR抑制物或样本中的细胞是否被带走,可有效防止假阴性情况。
主要部件
该试剂盒含有用于处理48项测试或质量控制的试剂,包括以下成分:
试剂A
| 姓名 | 主要组件 | 数量 |
| MPV检测 试剂 | 反应管中含有Mg2+, f3L基因/Rnase P引物探针, 反应缓冲液,Taq DNA酶。 | 48次测试 |
试剂B
| 姓名 | 主要组件 | 数量 |
| 多功能车 阳性对照 | 含有MPV靶片段 | 1管 |
| 多功能车 阴性对照 | 无 MPV 靶片段 | 1管 |
| DNA释放试剂 | 试剂含有Tris、EDTA 和 Triton。 | 48件 |
| 复溶试剂 | DEPC处理水 | 5毫升 |
注意:不同批号的组件不能互换使用
【储存条件和保质期】
1.试剂A/B可在2-30℃保存,保质期为10个月。
2.只有在准备进行测试时才打开试管盖。
3.请勿使用超过有效期的试管。
4.不要使用泄漏的检测管。
【适用文书】
适用于LC480 PCR分析系统、Gentier 48E全自动PCR分析系统、ABI7500 PCR分析系统。
【样品要求】
1.适用样品类型:咽拭子样本。
2.采样溶液:经验证,建议使用生理盐水或杭州特赛生物生产的病毒保存管进行样本采集。
咽拭子:用一次性无菌采样拭子擦拭双侧咽扁桃体及咽后壁,将拭子浸入含有3mL采样液的管中,弃去尾部,拧紧管盖。
3.样品的储存和运送:待测样品应尽快检测,运输温度保持在2~8℃。24小时内可检测的样品可保存在2~8℃,24小时内无法检测的样品应保存在≤-70℃(如无-70℃保存条件,可暂时保存在-20℃),避免重复检测。
冻结和解冻。
4.正确的样品采集、储存和运输对本产品的性能至关重要。
【测试方法】
1.样品处理及加样
1.1 样品处理
将上述上样溶液与样品混合后,取30μL样品放入DNA释放试剂管中,混匀。
1.2 装载
取20μL复溶试剂加入MPV检测试剂中,加入5μL上述处理好的样本(阳性对照、阴性对照需与样本同时处理),盖上管盖,2000rpm离心10秒。
2. PCR扩增
2.1 将准备好的PCR板/管装入荧光PCR仪,每次检测需设置阴性对照和阳性对照。
2.2 荧光通道设置:
1)选择FAM通道进行MPV检测;
2)选择HEX/VIC通道进行内参基因检测;
3.结果分析
将基线设置在阴性对照荧光曲线最高点上方。
4.质量控制
4.1 阴性对照:FAM、HEX/VIC通道未检测到Ct值,或Ct>40;
4.2 阳性对照:在FAM、HEX/VIC通道,Ct≤40;
4.3 同一次实验中应满足上述要求,否则测试结果无效,需重新进行实验。
【截止值】
当目标序列Ct≤40,内参基因Ct≤40时,判定样本为阳性。
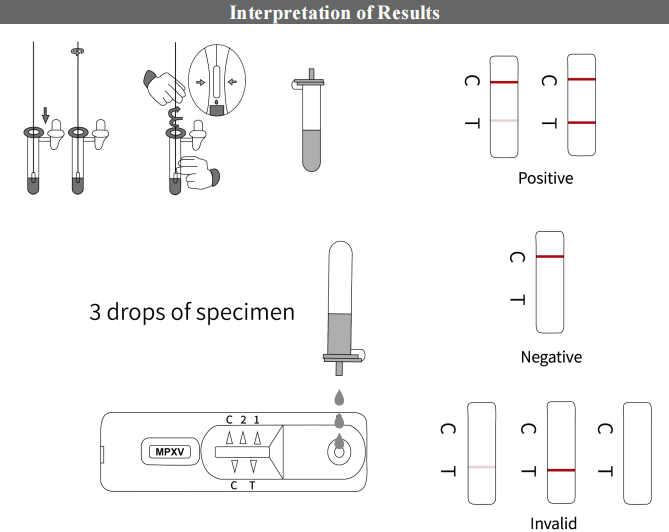
【结果解释】
质控通过后,用户需查看每个样本在HEX/VIC通道中是否有扩增曲线。若有,且Ct值≤40,则表明内控基因扩增成功,本次检测有效。用户可进行后续分析:
3.对于内控基因扩增失败的样本(HEX/VIC
通道、Ct>40或无扩增曲线)、病毒载量低或PCR抑制物的存在均可能是失败的原因,应从标本采集开始重新检查;
4.对于阳性样本及培养出的病毒,内控结果不影响;
对于检测结果为阴性的样本,内部控制需要检测结果为阳性,否则整体结果无效,需要从样本采集步骤开始重新检查
展览信息






公司简介
杭州特赛生物科技有限公司是一家快速发展的专业生物技术公司,专门研究、开发、制造和分销先进的体外诊断(IVD)检测试剂盒和医疗器械。
我们的工厂已通过GMP、ISO9001和ISO13458认证,并获得CE和FDA认证。我们期待与更多海外公司合作,共同发展。
我们生产的产品涵盖生育力检测、传染病检测、药物滥用检测、心脏标志物检测、肿瘤标志物检测、食品安全检测以及动物疾病检测等,其中,TESTSEALABS品牌已在国内外市场享有盛誉。凭借卓越的品质和优惠的价格,我们占据了国内市场50%以上的市场份额。
产品工艺

1.准备

2.封面

3.跨膜

4.切条

5.组装

6.打包袋子

7.密封包装袋

8.包装盒子

9.包装

预防新的悲剧:猴痘蔓延,立即做好准备
8月14日,世界卫生组织(WHO)宣布,猴痘疫情构成“国际关注的突发公共卫生事件”。这是自2022年7月以来,WHO第二次针对猴痘疫情发布最高级别警报。
目前,猴痘疫情已从非洲蔓延至欧洲和亚洲,瑞典、巴基斯坦等地均出现确诊病例。
据非洲疾控中心最新数据,今年以来,非洲联盟12个成员国共报告猴痘病例18737例,其中确诊病例3101例,疑似病例15636例,死亡病例541例,病死率为2.89%。
01 什么是猴痘?
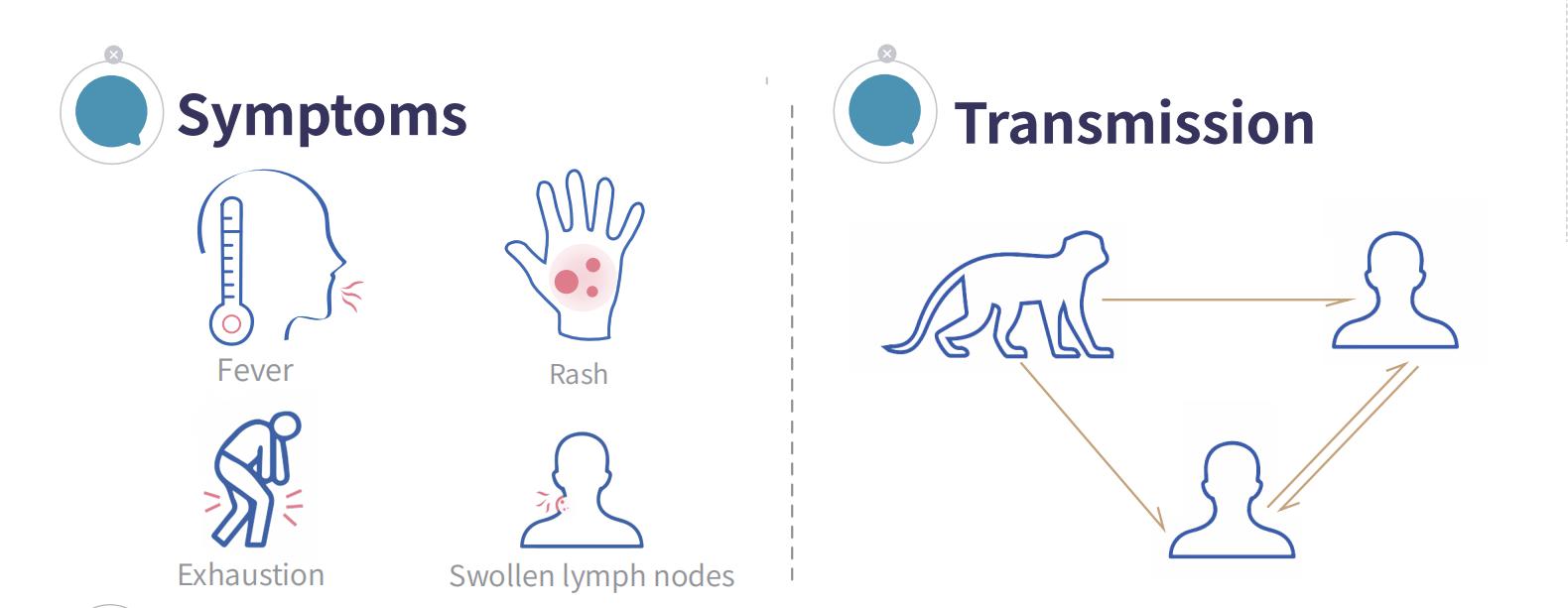
猴痘 (MPX) 是由猴痘病毒引起的一种病毒性人畜共患疾病。该病可在动物间传播,也可在人与人之间传播。典型症状包括发烧、皮疹和淋巴结肿大。
猴痘病毒主要通过黏膜和破损皮肤进入人体。传染源包括猴痘病例以及受感染的啮齿动物、猴类和其他非人类灵长类动物。感染后潜伏期为5至21天,通常为6至13天。
虽然一般人群对猴痘病毒易感,但由于两种病毒在基因和抗原性上相似,接种过天花疫苗的人对猴痘具有一定程度的交叉保护作用。目前,猴痘主要通过性接触在男男性行为者中传播,普通人群的感染风险仍然较低。
02 这次猴痘疫情有何不同?
自今年年初以来,猴痘病毒的主要毒株“Clade II”已在全球范围内引发大规模疫情。令人担忧的是,由病情更严重、死亡率更高的“Clade I”引起的病例比例正在上升,并且已在非洲大陆以外地区得到确认。此外,自去年9月以来,一种新的、更致命、更易传播的变种“Ib 支”的言论开始在刚果民主共和国蔓延。
此次疫情的一个显著特点是,妇女和15岁以下儿童受感染最为严重。
数据显示,报告病例中超过70%为15岁以下患者,在死亡病例中,这一数字上升至85%。值得注意的是,儿童的死亡率是成人的四倍。
03 猴痘传播的风险有多大?
由于旅游旺季和国际交往频繁,猴痘病毒跨境传播风险可能增加。但该病毒主要通过长时间密切接触传播,如性行为、皮肤接触、近距离呼吸或与他人交谈等方式传播,人际传播能力相对较弱。
04 如何预防猴痘?
避免与健康状况不明者发生性接触。旅客应关注目的地国家和地区的猴痘疫情,避免与啮齿动物和灵长类动物接触。
若出现高危行为,请自我监测健康状况21天,避免与他人密切接触。如出现皮疹、水疱、发热等症状,请及时就医,并告知医生相关行为。
如果家人或朋友确诊感染猴痘,请采取个人防护措施,避免与患者密切接触,不要接触患者使用过的物品,例如衣物、床上用品、毛巾和其他个人物品。避免共用浴室,并勤洗手和保持房间通风。
猴痘诊断试剂
猴痘诊断试剂通过检测病毒抗原或抗体,帮助确诊感染,从而采取适当的隔离和治疗措施,在控制传染病方面发挥着重要作用。目前,安徽深兰医疗科技有限公司已开发以下猴痘诊断试剂:
猴痘抗原检测试剂盒:采用胶体金法采集口咽拭子、鼻咽拭子或皮肤渗出液等样本进行检测,通过检测病毒抗原的存在来确诊感染。
猴痘抗体检测试剂盒:采用胶体金法,样本包括静脉全血、血浆或血清。通过检测人体或动物体内产生的针对猴痘病毒的抗体来确诊感染。
猴痘病毒核酸检测试剂盒:采用实时荧光定量PCR方法,样本为皮损渗出液,通过检测病毒基因组或特定基因片段来确诊感染。
Testsealabs 猴痘检测产品
自2015年以来,Testsealabs的猴痘诊断试剂已在国外实验室使用真实病毒样本进行验证,并因其稳定可靠的性能而获得CE认证。这些试剂针对不同类型的样本,提供不同的灵敏度和特异性水平,为猴痘感染检测提供强有力的支持,并更好地协助有效控制疫情。有关我们猴痘检测试剂盒的更多信息,请访问:https://www.testsealabs.com/monkeypox-virus-mpv-nucleic-acid-detection-kit-product/
测试程序
用棉签从脓疱中收集脓液,将其彻底混合在缓冲液,然后滴几滴到测试卡上。只需几个简单的步骤即可获得结果。