Testsealabs Krankheetstest TYP Typhus IgG/IgM Schnelltestkit
Schnell Detailer
| Markennumm: | Testsea | Produktnumm: | TYP Typhus IgG/IgM |
| Ursprungsplaz: | Zhejiang, China | Typ: | Ausrüstung fir pathologesch Analysen |
| Zertifikat: | ISO9001/13485 | Instrumentklassifikatioun | Klass II |
| Genauegkeet: | 99,6% | Exemplar: | Vollblutt/Serum/Plasma |
| Format: | Kassett/Sträif | Spezifikatioun: | 3,00mm/4,00mm |
| MOQ: | 1000 Stéck | Haltbarkeet: | 2 Joer |

Virgesinn Benotzung
Den Typhus IgG/IgM Schnelltest ass e Lateral-Flow-Immunoassay fir déi gläichzäiteg Noweisung an Differenzéierung vun Anti-Salmonella typhi (S. typhi) IgG an IgM am mënschleche Serum a Plasma. E soll als Screeningtest an als Hëllefsmëttel bei der Diagnos vun enger Infektioun mat S. typhi benotzt ginn. All reaktiv Prouf mam Typhus IgG/IgM Schnelltest muss mat alternativen Testmethoden bestätegt ginn.

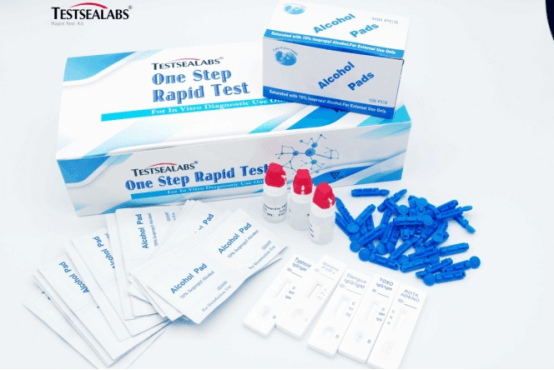
Resumé
Typhus gëtt duerch S. typhi, e gramnegativen Bakterium, verursaacht. Weltwäit ginn et all Joer geschätzte 17 Millioune Fäll a 600.000 Doudesfäll1. Patienten, déi mat HIV infizéiert sinn, hunn e wesentlech erhéichte Risiko fir eng klinesch Infektioun mat S. typhi2. Unzeeche vun enger H. pylori Infektioun stellen och e erhéicht Risiko duer fir Typhus ze kréien. 1-5% vun de Patienten ginn chronesch Träger a droen S. typhi an der Gallenblas.
Déi klinesch Diagnos vum Typhus hänkt vun der Isolatioun vun S. typhi aus Blutt, Knueweesmark oder enger spezifescher anatomescher Läsioun of. An Ariichtungen, déi sech dës komplizéiert an zäitopwänneg Prozedur net leeschte kënnen, gëtt de Filix-Widal-Test benotzt fir d'Diagnos ze erliichteren. Vill Aschränkungen féieren awer zu Schwieregkeeten bei der Interpretatioun vum Widal-Test3,4.
Am Géigesaz dozou ass den Typhus IgG/IgM Schnelltest en einfachen a schnelle Labortest. Den Test detektéiert an ënnerscheet gläichzäiteg d'IgG- an d'IgM-Antikörper géint S. typhi-spezifescht Antigen5t a Vollblutproben, wat hëlleft bei der Bestëmmung vun der aktueller oder fréierer Belaaschtung mat S. typhi.
Testprozedur
Loosst den Test, d'Prouf, de Puffer an/oder d'Kontrollen eng Raumtemperatur vun 15-30 ℃ (59-86 ℉) erreechen, ier Dir testt.
1. Bréngt d'Täsch op Raumtemperatur ier Dir se opmaacht. Huelt den Testgerät aus der Verpackung eraus.zouene Täsch a benotzt se sou séier wéi méiglech.
2. Leet den Testgerät op eng propper an gläichméisseg Uewerfläch.
3. Fir Serum- oder Plasmaprouf: Halt den Drëpse vertikal an transferéiert 3 Tropfen Serum.oder Plasma (ongeféier 100μl) an de Proufschacht(en) vum Testgerät, dann start denTimer. Kuckt d'Illustratioun hei ënnendrënner.
4. Fir Vollblutproben: Halt den Drëpse vertikal an transferéiert 1 Drëps Vollblut.Blutt (ongeféier 35 μl) an de Proufschacht (S) vum Testgerät, da gitt 2 Drëpse Puffer (ongeféier 70 μl) derbäi a start den Timer. Kuckt d'Illustratioun hei ënnendrënner.
5. Waart bis déi faarweg Linn(en) erschéngen. Liest d'Resultater no 15 Minutten. Interpretéiert d'Resultater net.Resultat no 20 Minutten.
Et ass essentiell, genuch Prouf ze benotzen, fir e gültegt Testergebnis. Wann d'Migratioun (d'Befeuchtung)vun der Membran) no enger Minutt net am Testfenster observéiert gëtt, füügt nach een Drëps Puffer derbäi(fir Vollblut) oder Prouf (fir Serum oder Plasma) an de Proufbrunn.
Interpretatioun vun de Resultater
Positiv:Zwee Linnen erschéngen. Eng Linn soll ëmmer an der Kontrolllinnregioun (C) erschéngen, aneng aner offensichtlech faarweg Linn sollt am Testlinnberäich erschéngen.
Negativ:Eng faarweg Linn erschéngt an der Kontrollregioun (C). Keng siichtbar faarweg Linn erschéngt and'Regioun vun der Testlinn.
Ongülteg:Kontrolllinn erschéngt net. Net genuch Proufvolumen oder falsch Prozedur.Techniken sinn déi warscheinlechst Ursaachen fir e Feeler an der Kontrollleitung.
★ Iwwerpréift d'Prozedur a widderhuelt seden Test mat engem neien Testgerät ausféieren. Wann de Problem bestoe bleift, stoppt direkt d'Benotzung vum Testkit a kontaktéiert Äre lokale Distributeur.
Informatiounen iwwer d'Ausstellung






Firmenprofil
Mir, Hangzhou Testsea Biotechnology Co., Ltd, sinn eng séier wuessend professionell Biotechnologiefirma, déi sech op d'Fuerschung, d'Entwécklung, d'Produktioun an d'Verdeelung vun fortgeschrattenen In-vitro-Diagnostik-Testkits (IVD) a medizineschen Instrumenter spezialiséiert huet.
Eis Ariichtung ass GMP-, ISO9001- an ISO13458-zertifizéiert a mir hunn eng CE- an FDA-Zoulassung. Mir freeën eis elo op d'Zesummenaarbecht mat méi auslännesche Firmen fir d'gemeinsam Entwécklung.
Mir produzéieren Fruchtbarkeetstester, Tester fir Infektiounskrankheeten, Drogenmëssbrauchstester, Häerzmarkertester, Tumormarkertester, Liewensmëttel- a Sécherheetstester an Déierekrankheetstester. Zousätzlech ass eis Mark TESTSEALABS souwuel am Inland wéi och am Ausland bekannt. Déi bescht Qualitéit a gënschteg Präisser erméiglechen et eis, iwwer 50% vun den Inlandsaktien ze iwwerhuelen.
Produktprozess

1. Virbereedung

2. Deckel

3. Kräizmembran

4. Sträif schneiden

5. Montage

6. Packt d'Täschchen

7. D'Täschchen zoumaachen

8. Packt d'Këscht

9. Ëmschloss