Testsealabs CEA Carcinoembryonic Antigen Test Kit
Parametertabell
| Modellnummer | TSIN101 |
| Numm | AFP Alpha-Fetoprotein Test Kit |
| Fonctiounen | Héich Empfindlechkeet, einfach, liicht a präzis |
| Exemplar | WB/S/P |
| Spezifikatioun | 3,0 mm 4,0 mm |
| Genauegkeet | 99,6% |
| Späicherung | 2°C-30°C |
| Versand | Iwwer Mier/Loft/TNT/FedEx/DHL |
| Instrumentklassifikatioun | Klass II |
| Zertifikat | CE ISO FSC |
| Haltbarkeet | zwee Joer |
| Typ | Ausrüstung fir pathologesch Analysen |
Prinzip vum FOB Rapid Testgerät
Den CEA-Schnelltestgerät (Vollblutt/Serum/Plasma) gouf entwéckelt fir mënschlecht karzinoembryonalt Antigen (CEA) duerch visuell Interpretatioun vun der Faarfentwécklung am internen Sträifen z'entdecken. D'Membran gouf mat Anti-CEA-Capture-Antikörper op der Testregioun immobiliséiert. Wärend dem Test gëtt d'Prouf mat faarwege kolloidalen Goldkonjugater vun Anti-CEA-monoklonalen Antikörper reagéiert, déi virum Proufpad vum Test beschichtet waren. D'Mëschung beweegt sech dann op der Membran duerch eng Kapillarwierkung an interagéiert mat Reagenzien op der Membran. Wann genuch CEA an de Prouwe sinn, bilt sech e faarwege Band an der Testregioun vun der Membran. D'Präsenz vun dësem faarwege Band weist e positivt Resultat un, während seng Feele e negativt Resultat uginn. D'Erscheinung vun engem faarwege Band an der Kontrollregioun déngt als prozedural Kontroll. Dëst weist datt de richtege Volumen vun der Prouf bäigefüügt gouf an d'Membranofzuch stattfonnt huet.

1. Maacht d'Foliebeutel net op, ier Dir prett sidd, mam Test unzefänken. Gekillt Testinstrumenter sollten op Raumtemperatur (15°-28°C) kommen, ier Dir d'Beutel opmaacht.
2. Huelt den Apparat aus der Schutztäsch a beschreift en mat der Proufidentifikatioun.
3. Füügt 50 µl frëscht Blutt an de Proufschacht (fir d'Kaart) oder de Proufpad (fir den Teststäbchen) bäi. Dann füügt 2 Drëpsen (50 µl) Testlaafpuffer an de Proufschacht oder de Proufpad bäi.
4. Liest d'Resultat bannent 10-15 Minutten. Liest d'Resultater net méi no 15 Minutten. Observéiert
dat faarwegt Band, dat sech iwwer der Kontrollregioun entwéckelt huet, weist drop hin, datt den Assay ofgeschloss ass.
Testprozedur
INHALT VUM KIT
1.Individuell verpackte Testgeräter
All Apparat enthält e Sträifen mat faarwege Konjugaten a reaktive Reagenzien, déi op déi entspriechend Regiounen virverdeelt sinn.
2.Wegwerfpipetten
Fir d'Zousätzlech vu Proben ze benotzen.
3.Puffer
Phosphatgepuffert Salzléisung a Konservéierungsmëttel.
4.Packungsbeilage
Fir d'Bedienungsinstruktioun.
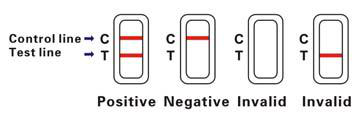
INTERPRETATIOUN VUN DE RESULTATER
Positiv (+)
Zwee rosa Sträifen erschéngen um Testberäich. Dëst weist drop hin, datt d'Prouf CEA enthält.
Negativ (-)
Nëmmen ee rosa Sträif erschéngt um Testberäich. Dëst weist drop hin, datt et kee CEA am Vollblut gëtt.
Ongülteg
Wann e faarwege Sträifen ouni Faarf um Testberäich erschéngt, ass dat en Hiwäis op e méigleche Feeler bei der Ausféierung vum Test. Den Test soll mat engem neien Apparat widderholl ginn.
Informatiounen iwwer d'Ausstellung






Firmenprofil
Mir, Hangzhou Testsea Biotechnology Co., Ltd, sinn eng séier wuessend professionell Biotechnologiefirma, déi sech op d'Fuerschung, d'Entwécklung, d'Produktioun an d'Verdeelung vun fortgeschrattenen In-vitro-Diagnostik-Testkits (IVD) a medizineschen Instrumenter spezialiséiert huet.
Eis Ariichtung ass GMP-, ISO9001- an ISO13458-zertifizéiert a mir hunn eng CE- an FDA-Zoulassung. Mir freeën eis elo op d'Zesummenaarbecht mat méi auslännesche Firmen fir d'gemeinsam Entwécklung.
Mir produzéieren Fruchtbarkeetstester, Tester fir Infektiounskrankheeten, Drogenmëssbrauchstester, Häerzmarkertester, Tumormarkertester, Liewensmëttel- a Sécherheetstester an Déierekrankheetstester. Zousätzlech ass eis Mark TESTSEALABS souwuel am Inland wéi och am Ausland bekannt. Déi bescht Qualitéit a gënschteg Präisser erméiglechen et eis, iwwer 50% vun den Inlandsaktien ze iwwerhuelen.
Produktprozess

1. Virbereedung

2. Deckel

3. Kräizmembran

4. Sträif schneiden

5. Montage

6. Packt d'Täschchen

7. D'Täschchen zoumaachen

8. Packt d'Këscht

9. Ëmschloss