Testsealabs サル痘ウイルス(MPV)核酸検出キット
使用目的
| アッセイタイプ | 咽頭ぬぐい液と鼻腔ぬぐい液 |
| テストの種類 | 定性 |
| 試験材料 | PCR |
| パックサイズ | 48テスト/1箱 |
| 保管温度 | 2~30℃ |
| 貯蔵寿命 | 10ヶ月 |
製品の特徴
原理
このキットは、MPV f3L遺伝子の特定の保存配列を標的領域としています。リアルタイム蛍光定量PCR技術と核酸迅速放出技術を用いて、増幅産物の蛍光シグナルの変化からウイルス核酸をモニタリングします。検出システムには内部品質管理機能が組み込まれており、サンプル中にPCR阻害物質が含まれているかどうか、またサンプル中の細胞が採取されているかどうかを監視することで、偽陰性を効果的に防止します。
主なコンポーネント
キットには、次のコンポーネントを含む 48 のテストまたは品質管理を処理するための試薬が含まれています。
試薬A
| 名前 | 主なコンポーネント | 量 |
| MPV検出 試薬 | 反応管にはMg2+が含まれており、 f3L遺伝子/RNase Pプライマープローブ、 反応バッファー、Taq DNA 酵素。 | 48件のテスト |
試薬B
| 名前 | 主なコンポーネント | 量 |
| MPV 陽性対照 | MPVターゲットフラグメントを含む | 1本 |
| MPV ネガティブコントロール | MPVターゲットフラグメントなし | 1本 |
| DNA放出試薬 | 試薬にはトリス、EDTAが含まれています そしてトリトン。 | 48個 |
| 再構成試薬 | DEPC処理水 | 5ML |
注: 異なるバッチ番号のコンポーネントは互換性がありません
【保管条件と賞味期限】
1.試薬A/Bは2~30℃で保存でき、保存期間は10ヶ月です。
2.試験の準備ができたら、試験管の蓋を開けてください。
3.使用期限を過ぎた試験管は使用しないでください。
4.漏れている検知管は使用しないでください。
【適用可能な機器】
LC480 PCR分析システム、Gentier 48E自動PCR分析システム、ABI7500 PCR分析システムに適しています。
【サンプル要件】
1.適用可能なサンプルの種類: 咽頭ぬぐい液サンプル。
2.サンプリング溶液:検証後、サンプル収集には、生理食塩水または杭州テストシーバイオロジー社製のウイルス保存チューブを使用することをお勧めします。
咽頭ぬぐい液:使い捨ての滅菌採取綿棒で両側の咽頭扁桃腺と後咽頭壁を拭き、綿棒を3mLの採取溶液が入ったチューブに浸し、綿棒の先端を捨ててチューブのカバーを締めます。
3.サンプルの保管と配送:検査対象となるサンプルはできるだけ早く検査する必要があります。輸送温度は2~8℃に保たれます。24時間以内に検査できるサンプルは2℃~8℃で保管できますが、24時間以内に検査できない場合は、-70℃以下(-70℃の保管条件がない場合は、一時的に-20℃で保管できます)で保管し、繰り返しの検査は避けてください。
凍結と解凍。
4. 適切なサンプルの収集、保管、輸送は、この製品のパフォーマンスにとって重要です。
【試験方法】
1.サンプル処理とサンプル追加
1.1 サンプル処理
上記のサンプリング溶液をサンプルと混合した後、サンプル30μLをDNA遊離試薬チューブに取り、均一に混合します。
1.2 読み込み
再構成試薬20μLをMPV検出試薬に加え、上記で処理したサンプル5μLを加え(陽性対照および陰性対照はサンプルと並行して処理する)、チューブのキャップを閉め、2000rpmで10秒間遠心分離する。
2. PCR増幅
2.1 準備したPCRプレート/チューブを蛍光PCR装置にセットし、各テストごとにネガティブコントロールとポジティブコントロールを設定します。
2.2 蛍光チャンネル設定:
1)MPV検出にFAMチャネルを選択します。
2)内部コントロール遺伝子検出にはHEX/VICチャネルを選択します。
3.結果分析
ベースラインをネガティブコントロールの蛍光曲線の最高点より上に設定します。
4.品質管理
4.1 ネガティブコントロール:FAM、HEX/VICチャンネルでCt値が検出されない、またはCt>40;
4.2 陽性対照:FAM、HEX/VICチャネルにおいて、Ct≤40;
4.3 上記の要件は同じ実験で満たされる必要があります。そうでない場合、テスト結果は無効となり、実験を繰り返す必要があります。
【カットオフ値】
サンプルは、ターゲット配列の Ct≤40、内部コントロール遺伝子の Ct≤40 のときに陽性とみなされます。
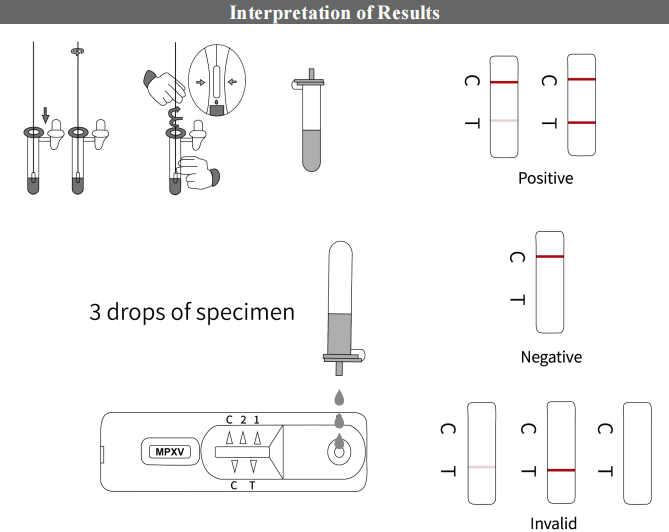
【結果の解釈】
品質管理に合格したら、HEX/VICチャンネルで各サンプルの増幅曲線を確認する必要があります。増幅曲線があり、Ct値が40以下の場合、内部コントロール遺伝子が正常に増幅され、この検査が有効であることが示されます。ユーザーはフォローアップ解析に進むことができます。
3.内部コントロール遺伝子の増幅に失敗したサンプル(HEX/VIC
PCR 阻害薬が陽性の場合、PCR チャンネルが 100 MHz 未満、Ct>40、または増幅曲線がないなど、ウイルス量が少ない、または PCR 阻害薬が存在することが失敗の理由である可能性があるため、検体採取から検査をやり直す必要があります。
4.陽性サンプルおよび培養ウイルスの場合、内部コントロールの結果は影響しません。
陰性の結果が出た場合、内部コントロールは陽性と判定される必要がある。そうでない場合、全体の結果は無効となり、検体採取段階から検査を繰り返す必要がある。
展示会情報






会社概要
私たち、杭州テストシーバイオテクノロジー株式会社は、高度な体外診断(IVD)検査キットと医療機器の研究、開発、製造、販売を専門とする、急成長中の専門的なバイオテクノロジー企業です。
当社の施設はGMP、ISO9001、ISO13458の認証を取得しており、CE、FDAの承認も取得しています。今後、より多くの海外企業と協力し、相互発展を目指してまいります。
当社は、不妊検査、感染症検査、薬物乱用検査、心筋マーカー検査、腫瘍マーカー検査、食品安全検査、動物疾患検査を製造しています。さらに、当社のブランドであるTESTSEALABSは、国内外の市場で高い評価を得ています。最高の品質と魅力的な価格設定により、国内シェアの50%以上を占めています。
製品プロセス

1.準備

2.カバー

3.膜を越える

4.ストリップを切る

5.組み立て

6.ポーチを詰める

7.袋を密封する

8.箱に詰める

9. ケース詰め

新たな悲劇を防ぐ:サル痘の蔓延に備えて今すぐ準備
8月14日、世界保健機関(WHO)は、サル痘の流行が「国際的に懸念される公衆衛生上の緊急事態」に該当すると発表しました。WHOがサル痘の流行に関して最高レベルの警戒レベルを発令したのは、2022年7月以来2度目となります。
現在、サル痘の流行はアフリカからヨーロッパ、アジアに広がっており、スウェーデンとパキスタンでも確認された症例が報告されている。
アフリカCDCの最新データによると、今年、アフリカ連合加盟12カ国で合計18,737件のサル痘症例が報告されており、うち確定症例は3,101件、疑い症例は15,636件、死亡者は541人で、致死率は2.89%となっている。
01 サル痘とは何ですか?
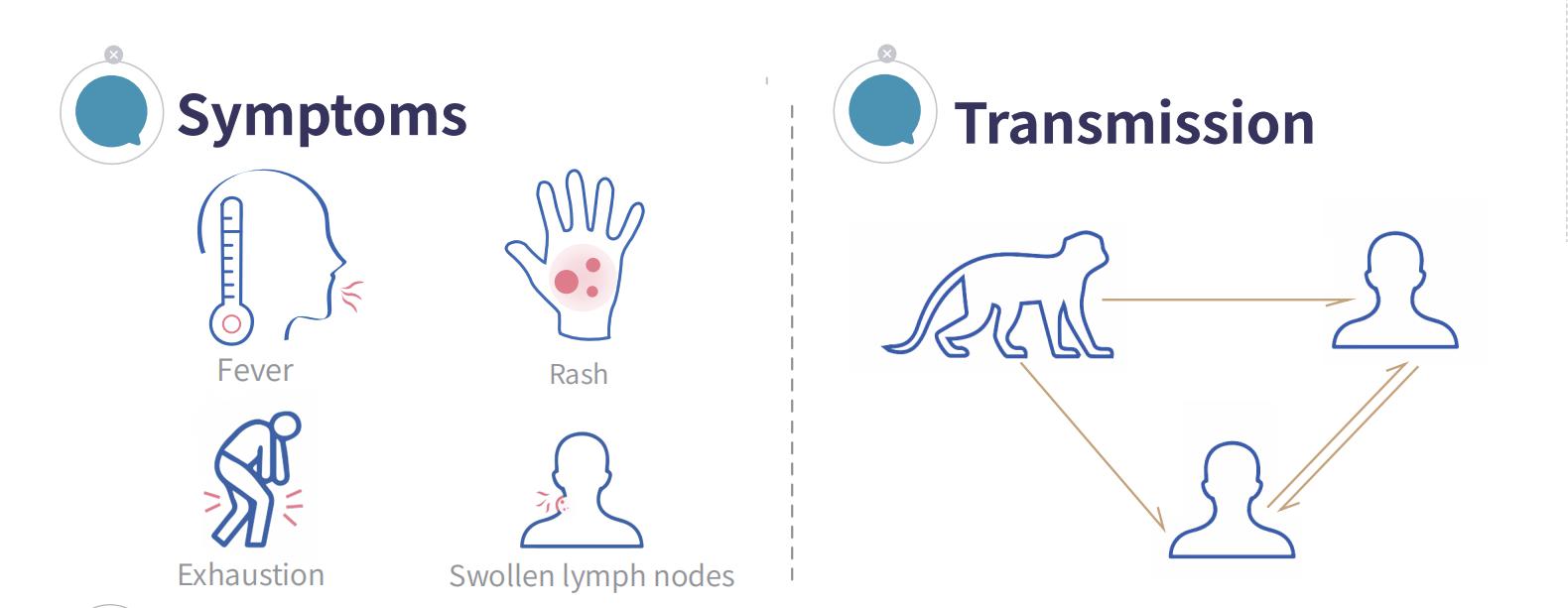
サル痘(MPX)は、サル痘ウイルスによって引き起こされるウイルス性人獣共通感染症です。動物から人間へ、また人間同士でも感染します。典型的な症状は、発熱、発疹、リンパ節腫脹などです。
サル痘ウイルスは主に粘膜や皮膚の損傷から人体に侵入します。感染源としては、サル痘患者、感染したげっ歯類、サル、その他のヒト以外の霊長類などが挙げられます。感染後、潜伏期間は5~21日、通常は6~13日です。
一般の人々はサル痘ウイルスに感染する可能性がありますが、天然痘ウイルスと天然痘ウイルスの遺伝的および抗原的類似性により、天然痘ワクチン接種を受けた人はサル痘に対してある程度の交差防御効果があります。現在、サル痘は主に男性同性愛者の間で性行為を通じて蔓延しており、一般の人々への感染リスクは低いままです。
02 今回のサル痘の流行は何が違いますか?
今年に入ってから、サル痘ウイルスの主流系統である「クレードII」が世界中で大規模な流行を引き起こしています。懸念されるのは、より重篤で致死率の高い「クレードI」による症例の割合が増加しており、アフリカ大陸以外でも確認されていることです。さらに、昨年9月以降、より致死性が高く、感染力の強い新たな変異株「クレードIb」がコンゴ民主共和国で広がり始めている。
この流行の注目すべき特徴は、女性と15歳未満の子供が最も影響を受けている点です。
データによると、報告された症例の70%以上が15歳未満の患者であり、死亡例においてはこの数字は85%に上ります。注目すべきは、子供の死亡率は大人の4倍高い。
03 サル痘感染のリスクはどれくらいですか?
観光シーズンや頻繁な国際交流により、サル痘ウイルスの国境を越えた感染リスクが高まる可能性があります。しかし、このウイルスは主に性行為、皮膚接触、至近距離での呼吸や会話など、長時間の濃厚接触によって感染するため、人から人への感染力は比較的弱いと考えられます。
04 サル痘を予防するには?
健康状態が不明な人との性行為は避けてください。旅行者は、渡航先の国や地域におけるサル痘の発生状況に注意し、げっ歯類や霊長類との接触を避ける必要があります。
リスクの高い行動をとった場合は、21日間健康状態を自己監視し、他の人との濃厚接触を避けてください。発疹、水疱、発熱などの症状が現れた場合は、速やかに医師の診察を受け、関連する行動について医師に報告してください。
家族や友人がサル痘と診断された場合は、個人防護措置を講じ、患者との濃厚接触を避け、患者が使用した衣類、寝具、タオルなどの私物に触れないようにしてください。また、浴室の共用を避け、こまめに手洗いを行い、部屋の換気を行ってください。
サル痘診断試薬
サル痘診断試薬は、ウイルス抗原または抗体を検出することで感染の確認に役立ち、適切な隔離・治療措置を可能にし、感染症の制御において重要な役割を果たします。現在、安徽省ディープブルー・メディカル・テクノロジー株式会社は、以下のサル痘診断試薬を開発しています。
サル痘抗原検査キット:金コロイド法を用いて、口腔咽頭スワブ、鼻咽頭スワブ、皮膚滲出液などの検体を採取し、ウイルス抗原の存在を検出することで感染を確認します。
サル痘抗体検査キット:金コロイド法を用い、静脈血、血漿、血清などの検体を採取します。ヒトまたは動物の体内でサル痘ウイルスに対して産生される抗体を検出することで感染を確認します。
サル痘ウイルス核酸検査キット:病変滲出液を検体として、リアルタイム蛍光定量PCR法を用いてウイルスのゲノムまたは特定の遺伝子断片を検出することで感染を確認します。
Testseabsのサル痘検査製品
2015年以来、Testsealabsのサル痘診断試薬は、海外の研究所で実際のウイルスサンプルを用いて検証され、その安定性と信頼性によりCE認証を取得しています。これらの試薬は様々なサンプルタイプを対象とし、幅広い感度と特異度レベルを提供することで、サル痘感染の検出を強力にサポートし、効果的なアウトブレイク制御を支援します。当社のサル痘検査キットの詳細については、https://www.testsealabs.com/monkeypox-virus-mpv-nucleic-acid-detection-kit-product/ をご覧ください。
テスト手順
綿棒を使って膿疱から膿を採取し、それをバッファーを数滴テストカードに塗布します。わずか数ステップで結果が得られます。