Kit de test rapide IgG/IgM pour la typhoïde Testsealabs
Détails rapides
| Nom de marque: | mer d'essai | Nom du produit: | TYP Typhoïde IgG/IgM |
| Lieu d'origine : | Zhejiang, Chine | Taper: | Équipements d'analyse pathologique |
| Certificat: | ISO9001/13485 | Classification des instruments | Classe II |
| Précision: | 99,6% | Spécimen: | Sang total/Sérum/Plasma |
| Format: | Cassette/Bande | Spécification: | 3,00 mm/4,00 mm |
| Quantité minimale de commande : | 1000 pièces | Durée de conservation : | 2 ans |

Utilisation prévue
Le test rapide IgG/IgM typhoïde est un test immunologique à flux latéral permettant la détection et la différenciation simultanées des IgG et IgM anti-Salmonella typhi (S. typhi) dans le sérum et le plasma humains. Il est destiné à être utilisé comme test de dépistage et comme aide au diagnostic de l'infection à S. typhi. Tout échantillon réactif au test rapide IgG/IgM typhoïde doit être confirmé par une ou plusieurs méthodes de test alternatives.

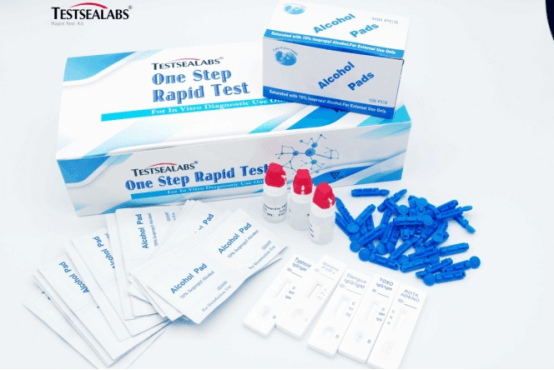
Résumé
La fièvre typhoïde est causée par S. typhi, une bactérie Gram négative. On estime que 17 millions de cas et 600 000 décès surviennent chaque année dans le monde. Les patients infectés par le VIH présentent un risque significativement accru d'infection clinique par S. typhi. La présence d'une infection à H. pylori augmente également le risque de contracter la fièvre typhoïde. 1 à 5 % des patients deviennent porteurs chroniques de S. typhi dans la vésicule biliaire.
Le diagnostic clinique de la fièvre typhoïde repose sur l'isolement de S. typhi dans le sang, la moelle osseuse ou une lésion anatomique spécifique. Dans les établissements ne pouvant se permettre cette procédure complexe et longue, le test de Filix-Widal est utilisé pour faciliter le diagnostic. Cependant, de nombreuses limitations rendent son interprétation difficile.
En revanche, le test rapide IgG/IgM typhoïde est un test de laboratoire simple et rapide. Il détecte et différencie simultanément les anticorps IgG et IgM dirigés contre l'antigène spécifique de S. typhi 5 dans un échantillon de sang total, facilitant ainsi la détermination d'une exposition actuelle ou passée à S. typhi.
Procédure de test
Laissez le test, l'échantillon, le tampon et/ou les contrôles atteindre la température ambiante de 15 à 30 °C (59 à 86 °F) avant le test.
1. Laisser le sachet revenir à température ambiante avant de l'ouvrir. Retirer le dispositif de test dusachet scellé et utilisez-le dès que possible.
2. Placez le dispositif de test sur une surface propre et plane.
3. Pour un échantillon de sérum ou de plasma : Tenez le compte-gouttes verticalement et transférez 3 gouttes de sérumou du plasma (environ 100 μl) dans le(s) puits d'échantillon du dispositif de test, puis démarrez leminuterie. Voir l'illustration ci-dessous.
4. Pour les échantillons de sang total : Tenez le compte-gouttes verticalement et transférez 1 goutte de sang totalVersez environ 35 μl de sang dans le(s) puits(s) du dispositif de test, puis ajoutez 2 gouttes de tampon (environ 70 μl) et démarrez le chronomètre. Voir l'illustration ci-dessous.
5. Attendez l'apparition des lignes colorées. Lisez les résultats après 15 minutes. N'interprétez pas lesrésultat après 20 minutes.
L'application d'une quantité suffisante d'échantillon est essentielle pour un résultat d'essai valide. En cas de migration (le mouillage)de la membrane) n'est pas observée dans la fenêtre de test après une minute, ajoutez une goutte supplémentaire de tampon(pour le sang total) ou l'échantillon (pour le sérum ou le plasma) dans le puits d'échantillon.
Interprétation des résultats
Positif:Deux lignes apparaissent. Une ligne doit toujours apparaître dans la zone de la ligne de contrôle (C), etune autre ligne colorée apparente devrait apparaître dans la zone de la ligne de test.
Négatif:Une ligne colorée apparaît dans la zone de contrôle (C). Aucune ligne colorée apparente n'apparaît dansla région de la ligne de test.
Invalide:La ligne de contrôle n'apparaît pas. Volume d'échantillon insuffisant ou procédure incorrecte.Les techniques sont les raisons les plus probables de la défaillance de la ligne de contrôle.
★ Revoyez la procédure et répétezEffectuez le test avec un nouveau dispositif. Si le problème persiste, cessez immédiatement d'utiliser le kit de test et contactez votre distributeur local.
Informations sur l'exposition






Profil de l'entreprise
Nous, Hangzhou Testsea Biotechnology Co., Ltd, sommes une société de biotechnologie professionnelle à croissance rapide spécialisée dans la recherche, le développement, la fabrication et la distribution de kits de tests de diagnostic in vitro (IVD) avancés et d'instruments médicaux.
Notre usine est certifiée BPF, ISO9001 et ISO13458, et bénéficie de l'agrément CE/FDA. Nous sommes impatients de collaborer avec d'autres entreprises étrangères pour un développement mutuel.
Nous produisons des tests de fertilité, des tests de maladies infectieuses, des tests de toxicomanie, des tests de marqueurs cardiaques et tumoraux, des tests de sécurité alimentaire et des tests de maladies animales. Notre marque TESTSEALABS est également reconnue sur le marché national et international. Notre excellente qualité et nos prix compétitifs nous permettent de détenir plus de 50 % des parts de marché nationales.
Processus de produit

1.Préparez

2.Couverture

3. Membrane croisée

4. Couper la bande

5. Assemblage

6.Emballez les sachets

7. Sceller les sachets

8.Emballez la boîte

9. Enveloppe