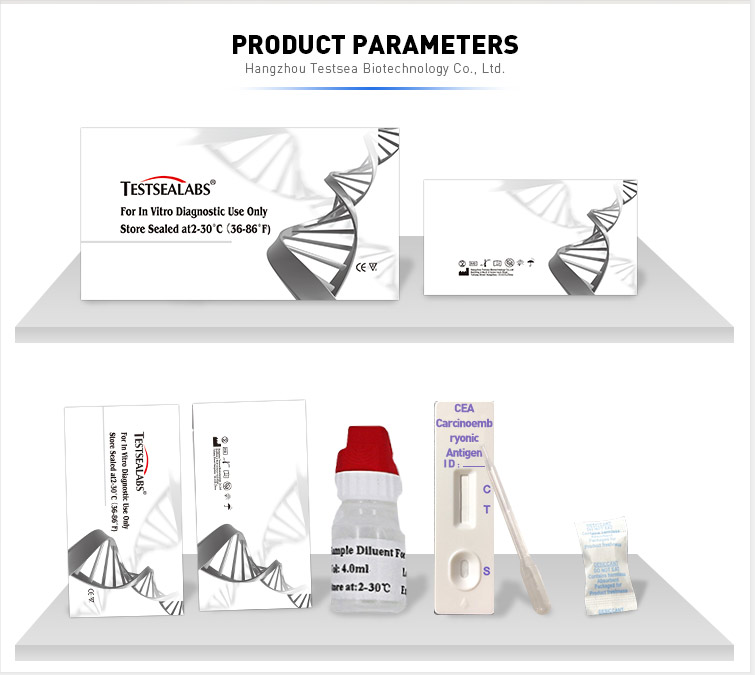
Kit de test d'antigène carcinoembryonnaire Testsealabs CEA
Tableau des paramètres
| Numéro de modèle | TSIN101 |
| Nom | Kit de test d'alpha-foetoprotéine AFP |
| Caractéristiques | Haute sensibilité, simple, facile et précis |
| Spécimen | WB/S/P |
| Spécification | 3,0 mm 4,0 mm |
| Précision | 99,6% |
| Stockage | 2°C-30°C |
| Expédition | Par mer/Par avion/TNT/Fedx/DHL |
| Classification des instruments | Classe II |
| Certificat | CE ISO FSC |
| Durée de conservation | deux ans |
| Taper | Équipements d'analyse pathologique |
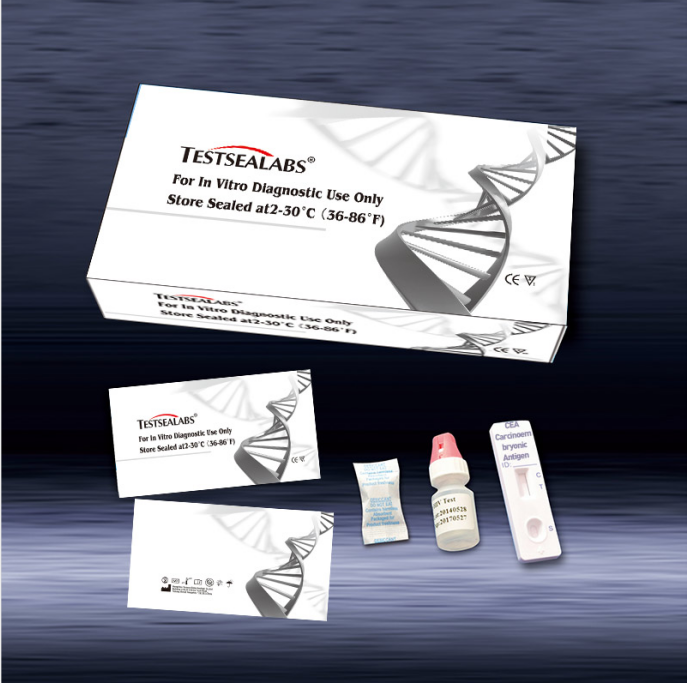
Principe du dispositif de test rapide FOB
Le dispositif de test rapide CEA (sang total/sérum/plasma) a été conçu pour détecter l'antigène carcinoembryonnaire humain (ACE) par interprétation visuelle de la coloration de la bandelette interne. La membrane a été immobilisée avec des anticorps de capture anti-ACE sur la zone de test. Pendant le test, l'échantillon réagit avec des conjugués d'or colloïdal d'anticorps monoclonaux anti-ACE colorés, pré-enduits sur le tampon échantillon. Le mélange se déplace ensuite sur la membrane par capillarité et interagit avec les réactifs présents. Si les échantillons contiennent suffisamment d'ACE, une bande colorée se forme sur la zone de test de la membrane. Sa présence indique un résultat positif, tandis que son absence indique un résultat négatif. L'apparition d'une bande colorée sur la zone de contrôle sert de témoin de procédure. Cela indique que le volume d'échantillon approprié a été ajouté et que la membrane a bien été absorbée.

1. N'ouvrez le sachet qu'au moment de commencer le test. Les dispositifs de test réfrigérés doivent être ramenés à température ambiante (15 à 28 °C) avant d'ouvrir le sachet.
2.Retirez l’appareil de la pochette de protection et étiquetez-le avec l’identification de l’échantillon.
3. Ajoutez 50 µl de sang frais dans le puits d'échantillon (pour la carte) ou dans le tampon d'échantillon (pour la jauge), puis ajoutez 2 gouttes (50 µl) de tampon de test dans le puits d'échantillon ou dans le tampon d'échantillon.
4. Lisez le résultat dans les 10 à 15 minutes. Ne lisez pas le résultat après 15 minutes. Observez
la bande colorée développée sur la région de contrôle indique que le test est terminé.
Procédure de test
CONTENU DU KIT
1.Dispositifs de test emballés individuellement
Chaque dispositif contient une bandelette contenant des conjugués colorés et des réactifs pré-étalés dans les régions correspondantes.
2.Pipettes jetables
Pour ajouter des spécimens, utilisez.
3.Tampon
Solution saline tamponnée au phosphate et conservateur.
4.Notice d'emballage
Pour les instructions d'utilisation.
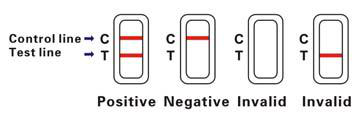
INTERPRÉTATION DES RÉSULTATS
Positif (+)
Deux bandes roses apparaissent sur la zone de test. Cela indique que l'échantillon contient de l'ACE.
Négatif (-)
Une seule bande rose apparaît sur la zone de test. Cela indique l'absence d'ACE dans le sang total.
Invalide
Si aucune bande colorée n'apparaît sur la zone de test, cela indique une possible erreur lors de la réalisation du test. Le test doit être répété avec un nouvel appareil.
Informations sur l'exposition






Profil de l'entreprise
Nous, Hangzhou Testsea Biotechnology Co., Ltd, sommes une société de biotechnologie professionnelle à croissance rapide spécialisée dans la recherche, le développement, la fabrication et la distribution de kits de tests de diagnostic in vitro (IVD) avancés et d'instruments médicaux.
Notre usine est certifiée BPF, ISO9001 et ISO13458, et bénéficie de l'agrément CE/FDA. Nous sommes impatients de collaborer avec d'autres entreprises étrangères pour un développement mutuel.
Nous produisons des tests de fertilité, des tests de maladies infectieuses, des tests de toxicomanie, des tests de marqueurs cardiaques et tumoraux, des tests de sécurité alimentaire et des tests de maladies animales. Notre marque TESTSEALABS est également reconnue sur le marché national et international. Notre excellente qualité et nos prix compétitifs nous permettent de détenir plus de 50 % des parts de marché nationales.
Processus de produit

1.Préparez

2.Couverture

3. Membrane croisée

4. Couper la bande

5. Assemblage

6.Emballez les sachets

7. Sceller les sachets

8.Emballez la boîte

9. Enveloppe